Desde el comienzo de la pandemia, se nos ha asegurado que el cumplimiento del enmascaramiento comunitario resolvería nuestros problemas y detendría la propagación del SARS-CoV-2. Sin embargo, los datos de aplicaciones del mundo real han demostrado consistentemente que fallan como medida de mitigación para la protección personal, y en lugar de corregir el curso de la guía aleatoria que se repartió, se nos dijo que máscara más fuerte con aparatos cada vez más restrictivos, aunque efectivamente no mitigadores.
Pero porque ¿Fracasaron y por qué siguen fallando? A continuación, profundizamos en los detalles de por qué, incluso suponiendo una hipotética capacidad de captura perfecta, los N95 no logran mitigar la propagación del SARS-CoV-2.
Deberíamos comenzar por ver la transmisibilidad viral y la producción de materia infecciosa como espectros, basados en la gravedad de la enfermedad, la respuesta inmunitaria de un individuo determinado y el progreso en el curso de la enfermedad. Se ha demostrado que todos estos tienen un impacto significativo en la carga viral de una persona infectada con SARS-CoV-2. Discutiremos las cifras de producción frente a las tasas de infectividad y los métodos de medición de la dosis infectiva mínima.
Cada uno de estos son factores importantes a considerar en la mitigación de patógenos, incluso de forma independiente, pero combinados, pueden mostrarnos específicamente si un enfoque dado tendrá el resultado deseado en la eliminación de un peligro infeccioso. Las cifras de salida de las emisiones respiratorias demuestran la cantidad de materia que expulsa un individuo y si son o no transmisibles con un patógeno respiratorio, pero las cifras de salida varían mucho entre las etapas más graves en el inicio de la enfermedad, los períodos de recuperación y cuando la PCR es negativa. para un patógeno dado.
Al comparar la salida con las proporciones de partículas a unidades formadoras de placa (PFU), se nos da una tasa de cuántas partículas emitidas son viriones viables capaces de causar infección. Cada una de estas unidades infecciosas se denomina PFU. El número de PFU que debe recibir un huésped potencial se proporciona como una cifra de dosis infectiva mínima (MID), que es un umbral que, una vez alcanzado, es de prever la aparición de la infección.
Al observar las cifras de la proporción de partículas a PFU y calcular el potencial MID, el producto final es la cantidad potencial de personas que pueden infectarse durante un período de tiempo determinado.
Con este umbral MID para el potencial de infectividad, podemos aplicar la capacidad de captura perfecta hipotética de un aparato determinado para ver si el mejor de los casos da como resultado la probabilidad de que el aparato mitigue o evite que se alcance el umbral MID para el peligro.
Aquí, analizamos la producción, la proporción de partículas a PFU y la MID para el SARS-CoV-2, en comparación con la hipotética capacidad de captura perfecta para los N95, para demostrar que incluso con una tasa perfecta de captura (y en este caso, de materia mucho más pequeña de lo que el aparato está aprobado o diseñado para capturar), el 5% por ciento nunca capturado sigue siendo una exposición potencial lo suficientemente abundante a la materia infecciosa como para provocar una infección.
Rangos de partículas y comportamiento correspondiente de la materia emitida
Las medidas de mitigación de la pandemia deberían haber comenzado con un tamaño de partícula mínimo viable, que para el SARS-CoV-2 cae entre 0.06 y 0.14 µm. Si bien los funcionarios de salud pública los presionan con frecuencia, los N95 están clasificados y aprobados únicamente para capturar materia de más de 0.3 µm. Se ha demostrado que más del 90 % de las partículas exhaladas caen bajo 0.3 µm. Este tamaño de materia permanece en el aire durante períodos prolongados: horas, incluso días, dependiendo de las tasas de intercambio de aire dentro del espacio dado. Se ha demostrado que el SARS-CoV-2 sigue siendo viable después de horas como aerosol fuera de un huésped y durante días en las superficies.
"El SARS-CoV-2 Se observó que el virus era viable durante 3 horas. en aerosoles, con disminución de la concentración de virus infecciosos de 103.5 al 102.7 TCID50 por litro de aire.”
Este estudio utilizó aerosoles generados en laboratorio que contenían SARS-CoV-2 infeccioso y observó la viabilidad de la materia emitida en diferentes superficies y como aerosoles a lo largo del tiempo.
Al considerar lo siguiente, uno también se pregunta si las membranas porosas de las máscaras y los respiradores jugaron un papel en el aumento del plazo de viabilidad de la materia viral:
"Los tiempos de supervivencia de virus aerotransportados en superficies diferir basado en si las superficies son no porosas (p. ej., plástico, acero inoxidable, vidrio) o porosas (p. ej., papeles y ropa). Las superficies no porosas son los principales contribuyentes a la transmisión de enfermedades, ya que se ha observado que los tiempos de supervivencia de los virus en el aire son mucho más largos que los de las superficies porosas”.
Las máscaras y los respiradores ciertamente cuentan como superficies porosas. Muchos respiradores también están construidos con plásticos fundidos por soplado. ¿Se ha estudiado suficientemente la viabilidad viral en las membranas de las mascarillas?
Las tasas de viabilidad de los aerosoles son importantes porque demuestran la capacidad de transmisión en espacios cerrados sin la presencia de un individuo transmisible. Con un individuo transmisible presente y emitiendo en el espacio dado, la salida sería constante, y la materia viral viable aumentaría la saturación atmosférica del patógeno por respiración.
Un problema crítico pero que se pasa por alto con las máscaras y los respiradores es el sellado: las pequeñas áreas de espacio hacen que estos aparatos sean ineficaces para el usuario. Rara vez, si alguna vez, alguien usa estos aparatos correctamente, bajo los términos de uso necesarios, por lo que nos encontramos con aparatos que ya no son mitigantes que se usan incorrectamente.
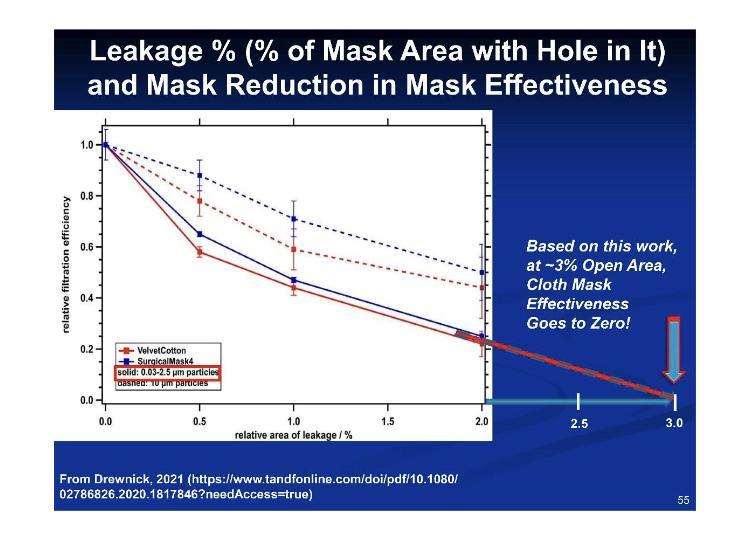
Según estas cifras de ajuste frente a fugas, un 3.2 % de fuga equivale a un 100 % de ineficacia.
Todos estos son factores que deben tenerse en cuenta al abordar la causa de que un aparato no mitigue un peligro determinado. Al examinar a continuación la producción de emisiones, la dosis infecciosa mínima, las unidades formadoras de placa y cómo se relacionan, podemos comprender mejor por qué los controles de ingeniería siempre fueron la respuesta correcta, no la implementación masiva de aparatos de protección respiratoria.
Emisiones respiratorias de pacientes "enfermos": resultados de prueba PCR positivos versus negativos:
En una investigación sobre la emisión de aerosoles en sujetos de prueba sanos frente a SARS-CoV-2 con PCR positivo, más del 90 % de las partículas emitidas por sujetos de prueba con PCR positivo fueron inferiores a 0.3 µm, y se realizaron recuentos de materia emitida comparando individuos con diferentes grados de enfermedad con sujetos PCR negativos.
"La mediana exhaló el conteo de partículas fue significativamente elevado en pacientes positivos para SARS-CoV-2 PCR (1490.5/L [46.0–34,772.0/L]) en comparación con los controles sanos (252.0/L [0.0–882.0/L]; p < 0.0001.”
Si usamos una tasa de emisión respiratoria de 4.3 a 29 litros por minuto (del Manual de factores de exposición de la EPA), el rango positivo de PCR de salida más alto de 34,772 29 partículas por litro multiplicado por 1,008,388 litros por minuto es tan alto como XNUMX XNUMX XNUMX partículas emitidas por minuto .
Si bien no estoy afirmando que todas esas partículas fueran partículas de virus individuales, o partículas de virus viables para el caso, existe una diferencia muy significativa en la materia emitida por individuos PCR positivos y negativos (valores medios de 1,490.5 frente a 252). Una relación para convertir partículas en PFU se presentará después de que se analice el papel de las PFU.
Tamaños de partículas y tasas de emisión:
El estudio discutió previamente las medidas, los rangos de tamaño de partículas emitidas en sujetos positivos y negativos para SARS-CoV-2.
"En cuanto a la partícula distribución de tamaño, los canales de tamaño disponibles (en total, 14 canales de tamaño de 0.15 a 5.0 μm) se analizaron en tres bandas de tamaño: <0.3 μm, 0.3–0.5 μm y >0.5–5.0 μm. Para ambos grupos, la mayoría de los aerosoles (>90 % en el grupo SARS-CoV-2 PCR positivo y >78 % en el grupo negativo) se encontraron en el rango más pequeño (<0.3 μm). Especialmente para el grupo positivo para COVID, los aumentos en la concentración total de aerosol estuvieron dominados por aumentos en partículas ≤0.3 μm”.
Diez individuos de los 64 pacientes hospitalizados muestreados, que se encontraban entre los casos más graves presentados, fueron responsables de alrededor del 64.8 % por ciento de los recuentos de partículas exhaladas, por lo que es importante en este caso observar menos rango de salida conservador y el potencial de infectividad cuando se ejecutan cálculos de salida y dosis infectiva mínima. Específicamente, el documento decía:
"En el SARS-CoV-2 El 15.6 % (n = 10/64) del grupo PCR positivo mostró recuentos altos y fue responsable del 64.8 % de todos los recuentos de partículas exhaladas en el grupo. Además, el 15.6 %, equivalente al 3.5 % de todos los pacientes (n = 10/288), fue responsable del 51.2 % de todas las partículas exhaladas”.
Si comparamos a aquellos que experimentan la mayor gravedad de la enfermedad con las tasas de infectividad, podemos entender más sobre la producción de partículas viables por parte de individuos transmisibles. Teniendo en cuenta la baja producción tanto de materia emitida como de viriones por parte de los sujetos de prueba con PCR negativa y recuperación de PCR positiva, puede ser seguro especular que habla de la baja probabilidad de que la transmisión asintomática sea un factor principal en la propagación viral.
La presencia de copias de ARN versus concentraciones de viriones viables
No todas las copias de ARN o partículas de virus son capaces de formar PFU que dan como resultado la replicación viral. Si bien se han proporcionado datos sobre cuántas unidades infecciosas se generan, esto es no la tasa de salida de emisiones. Estas son estimaciones de la producción viral total durante una infección.
"Dividiendo por estimaciones para el inverso de la tasa de eliminación viral da una producción total estimada de 3 × 109 a 3 × 1012 viriones, o 3 × 105 a 3 × 108 unidades infecciosas durante el curso completo de una infección característica”.
Simplificado, es una producción total de 3 mil millones a 3 billones de partículas de virus, o 300,000 300 a XNUMX millones de unidades infecciosas generadas durante el curso de la enfermedad.
Salida de virión
Hay diferentes métodos para establecer la producción de viriones, que ofrecen rangos ligeramente diferentes cuando se ven uno al lado del otro. Algunos estudios muestran el total de viriones emitidos, como los siguientes:
"Algunos pacientes tienen títulos virales que exceden el título promedio de Wölfel et al en más de dos órdenes de magnitud, lo que aumenta el número de viriones en las gotitas emitidas a más de 100,000 XNUMX por minuto de habla”.
Otros estudios brindan recuentos totales de partículas y se basan en el uso de factores de conversión de la producción total a viriones viables. Lo que es importante establecer es que la producción total de partículas de virus no es igual al total de viriones viables, es decir, viriones capaces de crear unidades formadoras de placas (PFU).
PFU: comprensión de las partículas de virus necesarias para formar unidades formadoras de placa (PFU) individuales:
Si bien todas las partículas virales y de ARN viral emitidas no son capaces de replicación viral y la creación de PFU, se entiende que cada PFU es creada por una partícula viral viable. Los siguientes extractos analizan el impacto de las PFU en las infecciones virales y su aparición.
"El ensayo está diseñado de modo que cada placa resulta de la infección al multiplicar una sola partícula de virus infeccioso. Como tal, PFU/ml se considera una medida del número de unidades infecciosas por mililitro (UI/ml), con la advertencia de que no se puede estar seguro de una relación uno a uno de placas a partículas infecciosas en la alícuota aplicada. ”
"Para la mayoría de los virus animales, una partícula infecciosa es suficiente para iniciar la infección”.
"La naturaleza lineal de la curva dosis-respuesta indica que un solo virión es capaz de iniciar una infección. Sin embargo, la alta proporción de partículas a pfu de muchos virus muestra que no todos los viriones tienen éxito. Una proporción alta de partículas a pfu a veces es causada por la presencia de partículas no infecciosas con genomas que albergan mutaciones letales o que han sido dañados durante el crecimiento o la purificación”.
"Generalmente se supone que una placa es el resultado de la infección de la célula por un solo virión. Si este es el caso, entonces todo el virus producido a partir del virus en la placa debería ser un clon, en otras palabras, debería ser genéticamente idéntico”.

Para resumir, una partícula viral viable, o virión, es capaz de crear una UFP, en la que esta partícula viral se replica. Parte de la materia creada es únicamente ARN viral incapaz de causar una infección de forma independiente, y parte de la materia creada es capaz de replicarse e infectarse.
La relación entre la producción total de partículas y la creación de PFU se denomina relación partícula a PFU. Para el SARS-CoV-2, la proporción de partículas emitidas a PFU es de 1000 a 1,000,000 XNUMX XNUMX.
Estudios de UFP y Dosis Infecciosa Mínima
Nuestra frecuencia respiratoria varía según la edad y el nivel de actividad. La frecuencia respiratoria humana promedio es de 16 a 20 respiraciones por minuto. Para los fines de esta discusión, se utilizará una tasa de respiración de 4.3 a 29 litros por minuto (del Manual de factores de exposición de la EPA). Esta referencia da un rango de hasta 53 litros por minuto. Analizaremos la producción como viriones por minuto y la dosis infectiva mínima como PFU y viriones para la transmisión, ya que ambos se exploran en la investigación disponible.
Datos de la Dosis Infecciosa Mínima (MID) de la Literatura:
Se han utilizado estudios de comparación de diferentes virus respiratorios y estudios en animales de SARS-CoV-2 para contribuir a muchas estimaciones de MID, pero este documento se centra únicamente en estudios en humanos tanto como sea posible.
"Aunque el MID del SARS-CoV-2 en humanos necesita más investigación, se espera que sean aproximadamente 100 partículas de virus. El único estudio en humanos con respecto a un coronavirus se ha informado para HCoV-229E y su MID es 9 PFU. Además, si la transmisión por aerosol es el modo dominante, entonces la MID sería más baja”.
"De hecho, infecciones basadas en aerosoles requieren menos dosis, por ejemplo, ~100 veces menos que las infecciones basadas en gotitas”.
"La dosis infectiva mínima de SARS-CoV-2 que causa COVID-19 en humanos en estudios transversales y de series de casos evaluados fue bajo; en un estudio de serie de casos que investigó la dosis infecciosa en 273 muestras de 15 pacientes positivos para SARS-CoV-2, la dosis infecciosa mínima detectada fue de 1.26 UFP in vitro en el ensayo COVID-19-RdRp/Hel.1 En otro estudio, 248 Se evaluaron muestras oro-nasofaríngeas de personas con COVID-19 y se informó que la dosis infecciosa era de 364 UFP”.
"En un estudio de serie de casos que evaluó a 97 niños de 10 años o menos, 78 niños de 11 a 17 años y 130 adultos, la dosis infecciosa en niños de 11 a 17 años fue menor que en otros dos grupos (125 UFP). Los niños tenían un crecimiento de virus vivo más bajo, umbrales de ciclo más altos y una concentración viral más baja en comparación con los adultos, por lo que los niños no son los principales portadores de la infección. Los niños de ⩽10 años tenían más probabilidades de ser asintomáticos que otros”.
"Uno de los más uno bien discutido (sic) es el estudio realizado por Basu et al., cuyo objetivo principal fue evaluar el tamaño de las gotas que tienen una alta probabilidad de causar infección. Pero además de este hallazgo, también tenían algunos puntos relacionados con la carga viral que puede causar la infección. Descubrieron que la cantidad de viriones que se colocan en la nasofaringe de un individuo muy cerca durante las 2.5 h de duración se aproxima a (11/5) viriones por minuto × 60 min × 2.5 h = 330".
Los estudios de comparación que incluyen otros coronavirus han demostrado que las PFU pueden ser bastante bajas para los virus respiratorios.
"Infectividad estimada de El SARS-CoV-1 fue comparable a otros coronavirus, incluido el HCoV-229E, un agente causante de un resfriado leve en humanos. ID10 e ID50 de SARS-CoV-1 se informaron como 43 y 280 PFU (400 TCID50) en un estudio experimental”.
"la identificación humana50 para el coronavirus estacional subtipo 229E que causa un resfriado común leve en humanos se informó que era 13 TCID50."
Las cifras discutidas en los estudios proporcionados sobre el SARS-CoV-2 fueron 1.26, 100, 125, 330 y 363 PFU para la transmisión, lo que nuevamente habla de un amplio espectro de susceptibilidad.
Producción de viriones viables versus potencial de umbral de dosis infectiva mínima
Al usar estas cifras disponibles, podemos abordar la afirmación de que los N95 brindan un valor protector significativo contra los aerosoles infecciosos al observar las contribuciones de salida, el potencial de infectividad de la materia viral emitida, los rangos de PFU, luego podemos sopesar estos rangos contra una hipotética capacidad de captura perfecta de los N95. capturando el 95% por ciento de la materia, frente al restante 5% por ciento no capturado. Una vez más, tenga en cuenta que los N95 no están diseñados ni aprobados para capturar <0.3 µm, y estamos hablando de un patógeno que tiene un tamaño de partícula mínimo viable de 0.06-0.14 µm.
Emisiones respiratorias de un individuo transmisible se ha demostrado que alcanza más de 100,000 750,000 viriones en un minuto, aunque no se puede suponer que todos los viriones emitidos sean infecciosos. Otros trabajos de investigación han afirmado una producción de hasta XNUMX viriones/minuto (pero faltan datos que respalden tales afirmaciones). También se debe tener en cuenta que, por supuesto, no inhalamos toda la materia expirada de un individuo, pero nuestra proximidad a un individuo transmisible, su tasa de salida, la duración dentro del espacio y la ventilación dentro de ese espacio dado son todos factores que tendrán un impacto en la probabilidad de transmisión que no puede expresarse de forma lineal o predecible.
En el estudio exploramos anteriormente, el rango positivo de PCR de mayor salida fue de 34,772 partículas por litro, y las que emitieron los rangos más altos de salida compusieron el 64% por ciento de la materia total emitida.
Primero, crearemos una salida por hora de cada uno de estos rangos, luego aplique la proporción de partículas a PFU para cada rango de 1,000 a 1,000,000.
Rango de salida A
Una hora de un individuo transmisible en un espacio cerrado emitiendo 100,000 viriones por minuto sería una salida de 6 millones de viriones (100,000×60 minutos). Un período de 8 horas en un espacio cerrado equivale a 48 millones de viriones emitidos (100,000 480 × 1,000 minutos). Con la proporción de partículas a PFU de 1,000,000 a 6,000, esto nos da 48,000 viriones viables en una hora, 8 en XNUMX horas.
Las cifras de UFP de los estudios discutidos que se proporcionaron fueron 1.26, 100, 125, 330 y 363 UFP requeridas como dosis infectiva mínima. Dividí cada cantidad de viriones viables por cada cifra de PFU para obtener cada potencial para el umbral MID enumerado.
Rango de salida B
En el estudio de recolección de partículas PCR-positivas, 34,772 partículas por litro fue el rango más alto recolectado, con ~64% por ciento del total de partículas emitidas y contadas provenientes de 10 fuentes que se encontraban entre las más afectadas por su infección con SARS-CoV-2 . Si observamos 34,772 partículas multiplicadas por un volumen de emisión de 29 litros por minuto, el rango de salida es tan alto como 1,008,388 partículas emitidas por minuto.
El Manual de exposición de la EPA enumera un rango por minuto de hasta 53 litros por minuto, por lo que usar una cifra de 29 litros por minuto no es el rango de producción más alto posible. Se utilizarán los rangos de producción de 7 y 29 litros por minuto porque son rangos de producción que caen en rangos de niveles de actividad sedentarios a moderados.
A 29 litros por minuto, multiplicado por 34,772 1,008,388 partículas por litro (60 60,503,280 1,008,388 partículas), para una duración de salida de 60 minutos, el producto es 484,026,240 8 1,008,388 (480 XNUMX XNUMX × XNUMX) partículas por hora y XNUMX XNUMX XNUMX por período de XNUMX horas (XNUMX XNUMX XNUMX × XNUMX minutos).
Con una proporción de partículas a PFU de 1,000 a 1,000,000 para COVID, esto nos da 60,503 viriones viables emitidos por hora y 484,026 viriones viables por período de 8 horas.
Estos cálculos nos brindan el potencial de salida de un individuo transmisible en términos no solo de cuántas partículas de virus se emiten, sino también del potencial para alcanzar el umbral MID para infectar a un número determinado de personas según la cifra de PFU que se utilice.
Si bien el rango de PFU demostrado para el SARS-CoV-2 es bastante amplio, debemos anticipar un espectro de transmisibilidad basado en el estado de salud individual y la respuesta inmunitaria. Si bien 1.26 PFU parece bastante bajo, se ha demostrado que el PFU para el SARS-Cov-1 es tan bajo como 13 PFU para alcanzar el umbral MID para el inicio de la infección.
Incluso si se usa una salida de emisiones más baja de 7 litros por minuto, eso da una tasa de 243,404 34,772 partículas por minuto (7 14,694,240 x 234,404)), 60 116,833,920 243,404 partículas por hora (480 8 x 1,000) y 1,000,000 1 14,604 (116,833 8 x XNUMX) partículas por XNUMX - Periodo de horas. Con una proporción de partícula a PFU de XNUMX a XNUMX aplicada, un período de una hora es una producción de XNUMX viriones viables y XNUMX en un período de XNUMX horas.

Con estos rangos de salida de intensidad sedentaria a moderada, muchas veces se alcanza el umbral MID para todas las cifras de PFU establecidas.
Por qué los N95 fallaron/están fallando/fallarán
Los respiradores con una clasificación N95 están diseñados y aprobados para capturar el 95 % de la materia sin base de aceite superior a 0.3 µm. El SARS-CoV-2 tiene un tamaño de partícula viable mínimo de 0.06-0.14 µm, muy por debajo del umbral de 0.3 µm, incluso si se une a una materia más grande, por lo que esta es una hipotética capacidad de captura perfecta para un rango de partículas para el que estos aparatos no están diseñados o aprobado para capturar, ni sus datos de aplicación han demostrado que se desempeñen al 95% o cerca de él.
A los efectos de un ejercicio de capacidad de captura perfecta hipotética, les concederemos un supuesto de tasa de captura perfecta del 95%. Si aplicamos el 5 % de las cifras MID demostradas en los rangos de salida A y B, se demostrará la infectividad de los viriones viables frente al 5 % por ciento nunca capturado (p. ej., sin fugas) si se obtiene una tasa perfecta hipotética del 95 % se cumple la captura.
Rango de salida A
Rango de salida B
29 litros por minuto
7 litros por minuto
Si asumimos una capacidad de captura perfecta hipotética para N95 de rangos de tamaño de partículas de materia que estos aparatos no están diseñados o aprobados para capturar, y aplicamos el 5% restante por ciento nunca capturado, la gran mayoría de los rangos de salida versus PFU requeridos para cumplir con MID El umbral todavía permite la exposición muchas veces el umbral MID para la infección potencial de muchas personas en períodos de 1 hora y 8 horas para cada rango establecido de salida.
Resumen
Nos relajamos con nuestros estándares de mitigación durante el brote de SARS-CoV-2 porque este patógeno no es mortal para la gran mayoría de las personas, con una tasa de supervivencia de alrededor del 99.8 %. Esta ligereza hacia una respuesta específica al peligro es increíblemente peligrosa cuando se aplica a patógenos y elementos de exposición más letales.
Al examinar el escenario hipotético del mejor de los casos, podemos predecir mejor si una medida dada tendrá un impacto de mitigación en el peligro identificado. Para N95 versus salida, proporciones de partículas a PFU y MID para SARS-CoV-2, el mejor de los casos de hipotética captura perfecta de materia que estos aparatos no están diseñados ni aprobados para capturar muestra que aún no son mitigantes para este peligro, y las recomendaciones para su uso deben ser reconsideradas inmediatamente.
Recursos adicionales:
Discute la carga viral promedio de las muestras: https://www.nature.com/articles/s41586-020-2196-x.
Dosis mínima infecciosa
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7090536/ (en MID en general, no en SARS-CoV-2 específico).
Glosario
aerosol- partículas dispersas en aire o gas, definidas como de menos de 5 micras de tamaño.
asintomático (propagación) – el concepto teórico de transmitir un patógeno a otros sin presentar ningún síntoma establecido de dicho patógeno.
saturación atmosférica - la cantidad de materia viable que permanece en el aire dentro de un espacio cerrado.
emisiones – materia respiratoria exhalada.
régimen de flujo laminar – partículas fluidas siguiendo caminos suaves en capas.
dosis infectiva mínima – la cantidad mínima de peligro a la que uno debe estar expuesto para poder anticipar la aparición de la enfermedad.
N95 - un respirador con filtro de partículas que no captura aceite capaz de bloquear hasta el 95 % de la materia por encima de 0.3 µm.
inicio - el comienzo de una enfermedad que se afianza una vez que se ha alcanzado el umbral mínimo de dosis infectiva.
producción - las emisiones que se liberan en un entorno dado por un individuo transmisible.
salida como una constante – un individuo dentro de un espacio cerrado que emite aerosoles respiratorios cargados de partículas infecciosas en la atmósfera dada, saturando más la atmósfera dada con materia infecciosa con cada respiración.
proporción de partículas a PFU – una relación para los cálculos de salida patógena que sopesa el número total de partículas emitidas frente a las partículas que son viablemente infecciosas.
PCR negativo – un sujeto de prueba dado no recibe un resultado de prueba positivo cuando se prueba con la metodología de PCR para un patógeno dado. PCR significa usar la técnica de reacción en cadena de la polimerasa.
PCR positivo – un sujeto de prueba dado recibe una prueba positiva cuando se prueba usando la técnica de reacción en cadena de la polimerasa para un patógeno dado.
capacidad de captura perfecta – captura de materia peligrosa a un porcentaje de eficacia equivalente proporcionado por un producto como su mejor tasa hipotética posible.
Unidades formadoras de placa (PFU) – la creación de PFU requiere que un virión infecte una célula huésped, donde comienza la replicación viral. Se requiere un umbral de un número dado de PFU para el inicio de la enfermedad, conocido como la dosis infectiva mínima.
copias de ARN - material genético requerido para hacer copias de proteínas dentro de una célula. Las copias de ARN no equivalen a viriones viables capaces de replicarse.
DICT50 – abreviatura de dosis infecciosa de cultivo de tejidos, que es la dilución de un virus necesaria para infectar el 50 % de las células en un ensayo de cultivo.
la carga viral - la cantidad de partículas de virus en una sustancia dada, emisión o dentro del cuerpo de un individuo transmisible.
viabilidad viral – viriones capaces de infectar una célula y crear unidades formadoras de placas (PFU).
virión o virión viable- una partícula completa de virus infeccioso.
Publicado bajo un Licencia de Creative Commons Atribución Internacional
Para reimpresiones, vuelva a establecer el enlace canónico en el original Instituto Brownstone Artículo y Autor.









